神经元干细胞 (NSC)、间充质干细胞 (MSC) 和诱导多能干细胞 (iPSC) 是目前用于AD研究的细胞之一。目前,有两种方法可用于治疗AD患者。第一个是刺激原生干细胞的产生,第二个是将干细胞移植到受损细胞或组织中以恢复它们。
用于AD的各种干细胞如图1
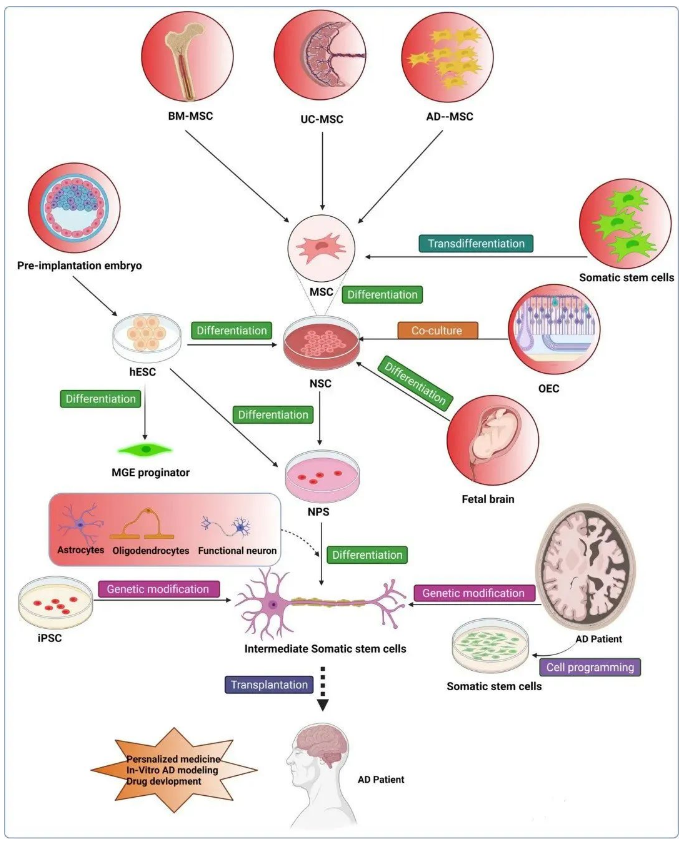
▲图片来源于网络 图1:各种干细胞用于对抗阿尔茨海默病。骨髓间充质干细胞、脐带间充质干细胞、人类胚胎干细胞、脂肪组织衍生间充质干细胞、诱导多能干细胞、神经干细胞、神经祖细胞,嗅鞘细胞,内侧神经节隆起样祖细胞,具有去除AD脑中淀粉样蛋白沉积的潜力。
神经干细胞在治疗AD中临床应用价值:成人大脑内的多能神经干细胞 (NSC) 存在于颗粒下区 (SGZ) 和脑室下区 (SVZ)。NSCs可以分化成细胞,包括神经元、少突胶质细胞和星形胶质细胞。NSCs可能还与ESCs和iPSCs、死后和胎儿新生儿脑组织不同或有区别。在动物AD模型中,移植的NSC被区分为发达的脑细胞形式。移植的细胞应分散在人造组织中以进行足够的神经元替代,然后将其引入宿主大脑的功能环境中。
NSC移植结束后获得的旁分泌结果确保了对细胞替代的鼓励,就像在其他干细胞中一样。为了挽救AD中的认知功能,从NSC发出的脑神经营养因子 (BDNF) 中获得显著。此外,据说NSC移植具有神经再生、神经保护和免疫调节作用。使用NSC移植的进一步研究保证了肿瘤发生和功能恢复。
间充质干细胞在治疗AD中的临床应用价值:作为多能细胞,间充质干细胞可以分化成多种细胞类型,如骨髓间充质干细胞(BMSCs)、脐带间充质干细胞(UC-MSCs)、脂肪来源间充质干细胞(AD-MSCs) , 和羊水MSCs (AF-MSCS)都是间充质干细胞中的一种。
间充质干细胞在治疗小鼠AD模型时,研究表明,UC-MSCs可以增加定期探索并有助于防止认知功能下降。间充质干细胞是应用最广泛的干细胞。因为与其他类型的干细胞相比,如果在标准交付之后获取 MSC,则相对容易选择和管理。与其他干细胞相比,MSCs也相对便宜,使其成为研究的有吸引力的选择。尽管存在伦理问题,但它们被用于许多 AD 研究项目,特别是生产性脐带血库,因为MSC具有最显著的再生潜力。
诱导多能干细胞在治疗AD中的优势:共有四种不同的转录因子,即OCT4、SOX2、c-MYC和KLF4,在产生诱导多能干细胞方面具有活性。每个转录因子负责一个特定的功能(iPSCs)。它们可以由异源人类细胞制成,可以发育成任何细胞,例如神经胶质细胞或神经元,因此可用于研究。
近年来,诱导多能干细胞(iPSC)被认为是一种很有希望的细胞疗法,可以在神经退行性疾病(如AD)中恢复大脑功能(Brookhouser et al. 2017)。为了评估iPSC对AD进展的潜在益处,我们立体定向注射小鼠iPSC衍生的神经前体(iPSC NPC)进入老年三重转基因(3xTg-AD)小鼠的海马,该小鼠具有广泛的AD典型病理异常(Armijo et al. 2021)。有趣的是,iPSC-NPCs移植小鼠表现出记忆改善、突触可塑性和AD脑病理学降低,包括淀粉样蛋白和缠结沉积减少。研究结果表明,iPSC-NPCs可能是一种有用的治疗方法,已用培养皿诱导多能干细胞疾病模型中的阿尔茨海默病已有明显效果(de Leeuw and Tackenberg 2019),可在AD的晚期临床和病理阶段产生益处。